Часто говорят, что рождение ребёнка — это чудо. Но если взглянуть на этот процесс с научной точки зрения, он оказывается ещё более удивительным. Представьте: два взрослых организма, мужчина и женщина, объединяют свои клетки, и в результате возникает новая жизнь, полностью свободная от признаков старения родителей. Эта начальная клетка начинает делиться с невероятной скоростью, порождая триллионы других, чтобы сформировать целый новый организм. Каждый из нас — звено в непрерывной цепи клеточных делений, тянущейся от одноклеточных предков, живших миллиарды лет назад. Сам процесс зарождения жизни — это и есть акт глубокого омоложения.
Секс — не единственный путь к вечной молодости
Принято считать, что омоложение возможно только через половое размножение, когда сливаются яйцеклетка и сперматозоид. Однако природа демонстрирует и другие, не менее эффективные стратегии. Некоторые организмы достигают своего рода «бессмертия» через клонирование. Яркий пример — тасманийский кустарник падуб королевский (Lomatia tasmanica). Он совершенно бесплоден, не даёт семян, а размножается исключительно вегетативно, черенками. Вся его популяция — это генетически идентичные клоны одного-единственного предка, который «жил» около 43 000 лет назад. Этот кустарник по сути клонирует себя уже десятки тысячелетий.
Грибы-гиганты и морские звёзды: мастера регенерации
Царство грибов также знает своих долгожителей. В Мичигане (США) растёт гриб опёнок тёмный, чей мицелий представляет собой единый организм возрастом около 2500 лет и весом в сотни тонн, занимающий 70 гектаров леса. А в Орегоне был обнаружен его ещё более внушительный собрат — опёнок толстоногий, чья грибница раскинулась на 880 гектаров и существует примерно 8500 лет. Учёные называют такие формы «грибами-монстрами» за их невероятные размеры и долголетие.
Способностью к омоложению через клонирование обладают и животные, например, морские звёзды. Если от звезды отрезать луч, из него может вырасти полноценная новая особь — точный генетический клон. Хотя морские звёзды также используют и половое размножение для ускорения эволюции, их вегетативный метод показывает, что природа изобрела множество способов обновления жизни без обязательного участия двух родителей.
Таким образом, идея о том, что всё в мире неизбежно стареет и умирает, подчиняясь энтропии, не совсем верна. Биология предоставляет примеры организмов, которые успешно противостоят старению, создавая молодые копии самих себя.
Метафора «Титаника»: кто спасётся в организме?
Представьте наше тело как корабль «Титаник», неумолимо движущийся к гибели — старению. Пассажиры на борту — это наши клетки. Лишь у немногих из них, «пассажиров первого класса», есть спасательные шлюпки. Это половые клетки (яйцеклетки и сперматозоиды), о которых эволюция заботится в первую очередь, ведь именно они отвечают за передачу генов следующим поколениям. Остальные 99% клеток организма — соматические — обречены и в конечном счёте погибнут вместе с «кораблём».
Но что, если мы сможем распространить привилегии «первого класса» на весь организм? Если научимся заимствовать у половых клеток и эмбрионов их механизмы омоложения и создадим внутри тела некое подобие равноправного «сообщества» клеток? Именно над этим вопросом бьётся современная наука о старении.

Предел Хейфлика и открытие Алексея Оловникова
Одним из главных препятствий на пути к вечной молодости считался так называемый предел Хейфлика. В 1951 году учёные обнаружили, что соматические клетки человека в лаборатории могут делиться лишь ограниченное число раз (около 40–60), после чего стареют и умирают. Казалось, это непреложный биологический закон старения.
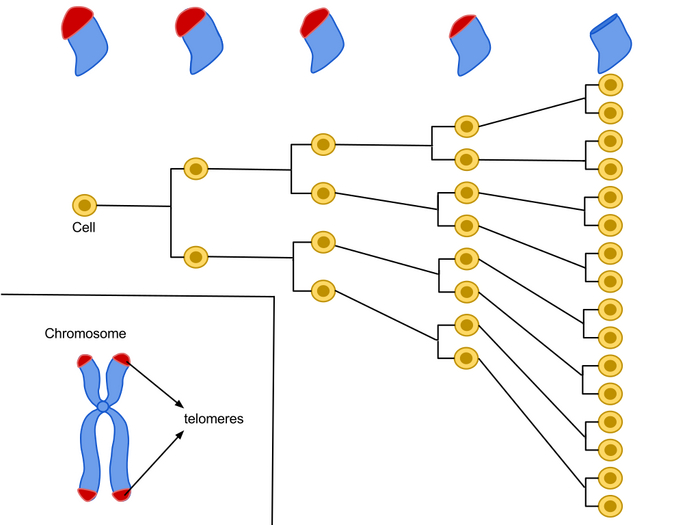
Однако ещё в 1971 году советский учёный Алексей Оловников обратил внимание на фундаментальную проблему копирования ДНК. При каждом делении клетки хромосомы немного укорачиваются на своих концах (теломерах), так как механизм репликации не может скопировать самые кончики молекулы. Оловников предположил, что должен существовать специальный механизм, восстанавливающий эти концы, и что именно их укорочение лежит в основе предела Хейфлика.
Теломераза: фермент молодости
Предсказание Оловникова блестяще подтвердилось в 1980-х годах, когда был открыт фермент теломераза. Его функция — достраивать укороченные теломеры, подобно тому как пластиковые наконечники шнурков защищают их от износа. Оказалось, что теломераза активна в «привилегированных» клетках: эмбриональных, стволовых и половых. Именно поэтому они могут делиться практически бесконечно, не старея.
Это открытие развеяло сомнения в возможности клонирования. Когда была клонирована овечка Долли из взрослой клетки, многие скептики считали, что её теломеры будут короткими, и она быстро состарится. Однако в процессе клонирования в эмбрионе активировалась теломераза, и теломеры восстановились до нормальной длины, дав жизнь здоровому ягнёнку.
Важность теломеразы для здоровья подчёркивают и генетические болезни, например, врождённый дискератоз, при котором теломеры укорачиваются катастрофически быстро. Больные стремительно стареют, у них развиваются тяжёлые заболевания, и продолжительность жизни резко сокращается.
Эксперименты на мышах: первые успехи
Идея активировать теломеразу для борьбы со старением столкнулась с серьёзным опасением: этот же фермент активен в раковых клетках, помогая им бесконтрольно делиться. Учёные опасались, что продление теломер спровоцирует онкологические заболевания.
Чтобы проверить эту гипотезу, были созданы генетически модифицированные мыши с повышенной активностью теломеразы и одновременно с усиленными противораковыми генами. Результаты оказались обнадёживающими: продолжительность жизни таких мышей увеличилась на 9–20%, а в комбинации с другими генами — до 40%. При этом риск рака не только не вырос, но в некоторых экспериментах даже снизился. Другое исследование показало, что мыши, просто рождённые с длинными теломерами, живут на 10% дольше и также меньше подвержены раку.
Генная терапия: путь к человеку?
Поскольку люди не рождаются с активированной теломеразой во всех клетках, учёные исследуют методы генной терапии. Взрослым мышам вводили вирус, несущий ген теломеразы. Это продлевало им жизнь на 10–20% без увеличения заболеваемости раком. Более совершенный самовоспроизводящийся вирусный вектор дал ещё более впечатляющий результат — увеличение жизни более чем на 40%.
Этот подход обнадёживает своей потенциальной доступностью. Технология доставки гена в клетку с помощью вирусной оболочки аналогична той, что используется в некоторых современных вакцинах (например, «Спутник V»). Теоретически, «прививка молодости» на основе теломеразы могла бы стать столь же массовой и недорогой.
Второй ключ: эпигенетический сброс
Однако одного удлинения теломер недостаточно. Другой важный фактор старения — эпигенетические изменения. Это «метки» на ДНК, которые включают или выключают гены в разных типах клеток. С возрастом эти метки «сбиваются», что приводит к нарушению работы клеток.
К счастью, этот процесс обратим. Внутри эмбриона происходит полный эпигенетический сброс — возврат к исходным «заводским настройкам». Воспроизвести это открыл японский учёный Синъя Яманака. Он показал, что введение всего четырёх генов (факторов Яманаки) во взрослую клетку может превратить её обратно в эмбриональную стволовую клетку. Это открытие, удостоенное Нобелевской премии, дало инструмент для омоложения клеток на эпигенетическом уровне.
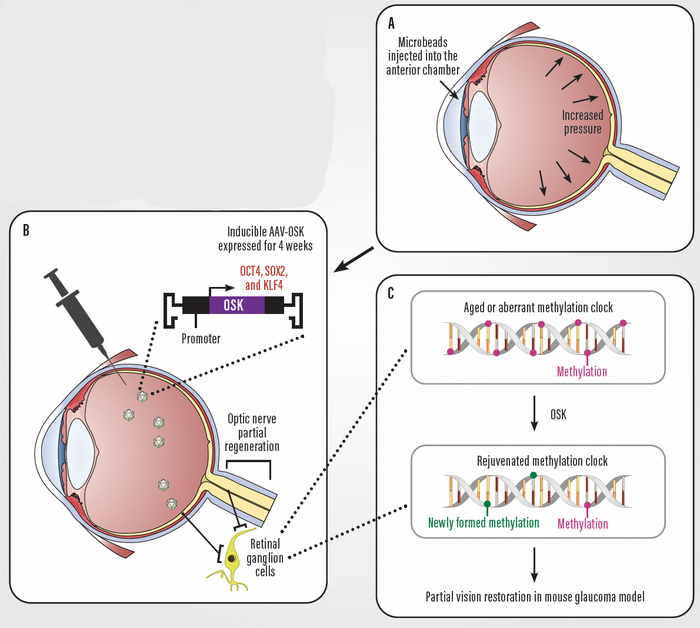
Сейчас учёные ищут способы безопасно и контролируемо применять факторы Яманаки в целом организме, чтобы не превратить его в бесформенную массу клеток. Эксперименты на мышах уже показали, что кратковременная активация этих генов может частично обратить вспять старение и даже восстановить зрение у животных с глаукомой. Это направление считается крайне перспективным и привлекает крупные инвестиции, например, от основателя Amazon Джеффа Безоса.
Третий ключ: уборка клеточного мусора
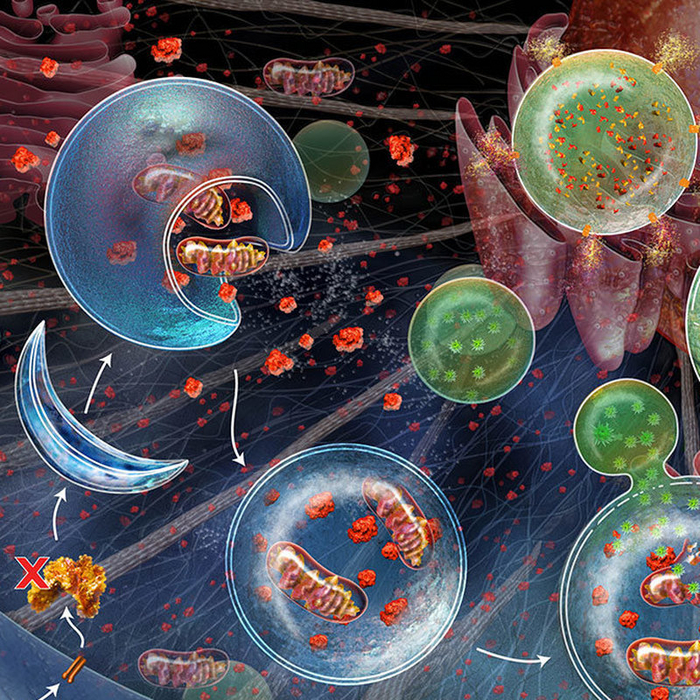
С возрастом в клетках накапливается «мусор»: повреждённые белки, органеллы и, что особенно важно, неисправные митохондрии («энергостанции» клетки). Для их утилизации существует процесс аутофагии — своеобразная система внутренней очистки. В эмбрионе эта система работает на полную мощность, избавляя новую жизнь от всего накопленного «груза».
Особую опасность представляют дефектные митохондрии, которые, в отличие от другого мусора, могут размножаться. Для их удаления существует специальный процесс — митофагия. Он работает как система контроля качества: на поверхности повреждённых митохондрий накапливается белок PINK1, который, в свою очередь, привлекает белок PARKIN. Это служит сигналом для клетки: «эту митохондрию нужно уничтожить».
Сбои в этой системе, например, мутации в генах PINK1 или PARKIN, приводят к накоплению плохих митохондрий в нейронах мозга и являются одной из причин развития болезни Паркинсона. Таким образом, поиск лекарств от этой болезни может открыть путь к улучшению очистки клеток у здоровых людей и продлению их жизни.
Четвёртый ключ: ремонт ДНК
Наконец, последний барьер на пути к долголетию — накопление мутаций в ДНК. Хотя в клетках существуют сложные системы репарации (починки) ДНК, с возрастом их эффективность падает. Особенно хорошо эти системы работают в половых клетках, что логично с точки зрения эволюции: важно передать потомству неповреждённые гены.
Один из ключевых белков в этой системе — ATM, который обнаруживает повреждения ДНК и запускает их исправление. У людей с неработающим геном ATM развивается синдром Луи-Бар — заболевание, сопровождающееся ускоренным старением и высоким риском рака. Учёные предполагают, что усиление систем репарации ДНК в соматических клетках до уровня, характерного для половых, могло бы значительно продлить здоровье наших органов.
Заключение: общая стратегия
Итак, современная наука выделяет несколько основных направлений борьбы со старением, подсказанных самой природой и процессами, происходящими в эмбрионах:
- Удлинение теломер с помощью активации теломеразы.
- Эпигенетический сброс с использованием факторов Яманаки.
- Очистка от клеточного мусора через усиление аутофагии и митофагии.
- Улучшение репарации ДНК для борьбы с мутациями.
Каждое из этих направлений уже показало promising результаты в экспериментах на животных. Главная задача будущего — научиться безопасно и точно применять эти механизмы в организме человека, по сути «отобрав привилегии» у половых клеток и распространив их на всё тело. Путь к радикальному продлению здоровой жизни лежит через глубокое понимание и заимствование тех «чудес», которые природа уже миллиарды лет использует для создания и обновления жизни.
Рекомендации ↗
[my]Научная поп-музыкаНаучные исследованияЭволюционная биологияГенетикаАлександр ПанчинУченыйНаукаПроДНКСтарениеОмоложениеБессмертиеВидеоYouTubeДлинные посты 20Больше интересных статей здесь: Новости науки и техники.
Источник статьи: Невероятное чудо бессмертия: тайны эмбрионов.

