Революционное открытие в молекулярной биологии переворачивает устоявшиеся представления: клеточное ядро, которое долгое время считалось метаболически пассивным, на самом деле активно участвует в защите генома. В ответ на повреждения ДНК ядро мобилизует антиоксидантные ферменты для срочного восстановления генетического материала. Это фундаментальное изменение в понимании клеточных процессов открывает путь к разработке принципиально новых и более эффективных методов борьбы с раком.
Окислительный стресс и постоянная угроза для ДНК
Внутри наших клеток кипит жизнь: непрерывные метаболические реакции превращают питательные вещества в энергию и строительные блоки. Однако этот процесс имеет побочный эффект — образование активных форм кислорода (АФК), таких как перекись водорода. Эти соединения действуют подобно ржавчине, повреждая структуру ДНК. Генетический материал постоянно атакуется как внутренними (эндогенными), так и внешними (экзогенными) мутагенами.
Сложная система защиты генома
Для противодействия окислительному стрессу клетки запускают многоуровневую систему защиты. Антиоксидантные ферменты обезвреживают АФК прямо у источника их возникновения, а на каждом участке хроматина запускаются специфические реакции репарации. Если повреждения слишком серьезны, клетка может временно остановить свой цикл, чтобы сосредоточиться на починке ДНК, или даже инициировать апоптоз — запрограммированную гибель, чтобы не допустить распространения мутаций. Эта стратегия защищает 3 миллиарда нуклеотидов в каждой клетке, предотвращая развитие болезней и врожденных аномалий.
До недавнего времени наука полагала, что вся метаболическая активность, связанная с энергетическим обменом и защитой генома, сосредоточена вне ядра — в цитоплазме и митохондриях. Ядро же считалось относительно пассивным хранилищем генетической информации. Новое исследование, опубликованное в журнале «Молекулярная системная биология», опровергает эту догму.
Обратите внимание: Обновление Windows 10 в октябре приостановлено, оно вызывает слишком много проблем.
Ядро заимствует митохондриальный механизм
Ученые из Центра геномной регуляции в Барселоне и Медицинского университета Вены сделали сенсационное открытие. Оказалось, что при обширном повреждении ДНК ядро активизируется и «импортирует» механизм восстановления из митохондрий. Это доказывает, что ядро метаболически активно. Поскольку раковые клетки часто перестраивают клеточный метаболизм для своего роста, это открытие дает ценнейшие подсказки для создания более прицельных противоопухолевых терапий.
Эксперимент, изменивший представления
Чтобы изучить процесс в деталях, исследователи смоделировали повреждение ДНК в человеческих клетках in vitro с помощью этопозида — распространенного химиотерапевтического препарата. Этот препарат повреждает ДНК раковых клеток, блокируя ферменты репарации, что в итоге приводит к их гибели.
К удивлению ученых, повреждение ДНК вызвало накопление АФК непосредственно в ядре. Более того, ферменты клеточного дыхания — основного источника АФК — начали перемещаться из митохондрий в ядро, чтобы участвовать в починке генетического материала.
«Где дым, там и огонь, а где активные формы кислорода, там работают метаболические ферменты, — поясняет Сара Сдельчи, руководитель исследования. — Наша работа демонстрирует существование особого типа метаболизма, который локализован именно в ядре».
Ключевым игроком в этом процессе оказался фермент PRDX1, который обычно функционирует в митохондриях. При повреждении ДНК клетка «приказывает» ему мигрировать в ядро. Там PRDX1 не только помогает восстановить ДНК, но и повышает доступность аспартата — важнейшего компонента для синтеза нуклеотидов. Это первый случай, когда подобный механизм был зафиксирован на ядерном уровне.
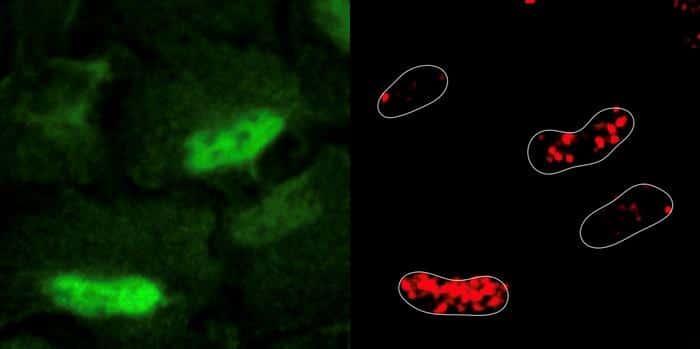
На изображении показан участок повреждения ДНК (зеленый) и фермент PRDX1 (красный), который его восстанавливает.
Новые горизонты в терапии рака
Используя технологию редактирования генов CRISPR-Cas9, ученые выявили гены, критически важные для выживания клеток. Оказалось, что «отключение» генов, отвечающих за клеточное дыхание, делает здоровые клетки устойчивыми к этопозиду. Это объясняет ограниченную эффективность подобных препаратов против многих опухолей: раковые клетки часто переходят на гликолиз (бескислородный метаболизм) и могут обходиться без клеточного дыхания.
Эти данные указывают на перспективные направления для разработки терапии. Например, комбинация этопозида с препаратами, стимулирующими выработку АФК, могла бы преодолеть устойчивость опухолей к химиотерапии. Другой подход — использование ингибиторов синтеза нуклеотидов, которые помешали бы раковым клеткам ремонтировать свою ДНК, что привело бы к их гибели.
Больше интересных статей здесь: Новости науки и техники.
Источник статьи: В случае повреждения ядро клетки вызывает антиоксидантные ферменты для восстановления ДНК и сохранения целостности генома.

